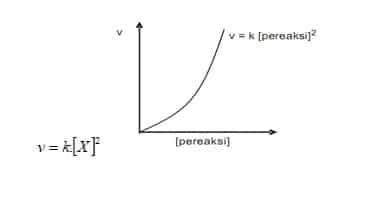
Laju reaksi menyatakan molaritas zat terlarut dalam reaksi yang dihasilkan tiap detik reaksi. Persamaan laju reaksi merupakan persamaan aljabar yang menyatakan hubungan laju reaksi dengan konsentrasi pereaksi.

76691693 Laporan Praktikum Fisiologi Tumbuhan
Contoh laporan praktikum laju reaksi. Pengertian faktor yang mempengaruhi dan rumus beserta contoh soalnya lengkap konsep pembelajaran kimia merupakan konsep yang erat dengan kehidupan sehari hari. Pengaruh konsentrasi terhadap laju reaksi praktikum kimia contoh soal pembahasan laju reaksi dari berbagai reaksi biasanya berbeda beda ada yang cepat dan ada yang lambat. Laju sesaat adalah laju pada saat tertentu. Sebagai telah kita lihat sebelumnya laju reaksi berubah dari waktu ke waktu. Contoh laporan praktikum kimia. Pada praktikum kali ini telah dilakukan percobaan mengenai faktor faktor yang mempengaruhi laju reaksi.
Salah satu faktor yang mempengaruhi laju reaksi di antaranya adalah konsentrasi pereaksi. Laju reaksi dipengaruhi oleh luas permukaansemakin besar luas permukaan zat padat yang direaksikan semakin lambat laju reaksinyanamunsemakin kecil luas permukaan zat padat yang direaksikan semakin cepat laju reaksi yang terjadi. Kimia menggambarkan kehidupan sedemikian rupa sehingga. Perkaratan besi merupakan contoh reaksi kimia yang berlangsung lambat sedangkan peledakan mesiu atau kembang api adalah contoh reaksi yang cepat. Serta kita dapat mempelajari jenis reaksi kimia diantaranya yaitu reaksi penggabungan reaksi penguraian reaksi penggantian reaksi penggantian rangkap dan reaksi netralisasi. Laju reaksi adalah laju penurunan reaktan pereaksi atau laju bertambahnya produk hasil reaksi.
Oleh karena itu plot konsentrasi terhadap waktu berbentuk garis lengkung seperti gambar di bawah ini. Laju reaksi atau kecepatan reaksi menyatakan banyaknya reaksi kimia yang berlangsung per satuan waktulaju reaksi menyatakan molaritas zat terlarut dalam reaksi yang dihasilkan tiap detik reaksi. Pada umumnya laju reaksi makin kecil seiring dengan bertambahnya waktu reaksi. Perubahan reaksi kimia sangat penting karena merupakan kemampuan dasar untuk praktikum praktikum selanjutnya. Pada percobaan pertama dilakukan pengamatan faktor laju reaksi yaitu konsentrasi yang dilakukan dengan mereaksikan pita magnesium bersama hcl yang konsentrasinya berbeda beda. Perkaratan besi merupakan contoh reaksi kimia yang berlangsung lambat sedangkan peledakan mesiu atau kembang api adalah contoh reaksi yang cepat.
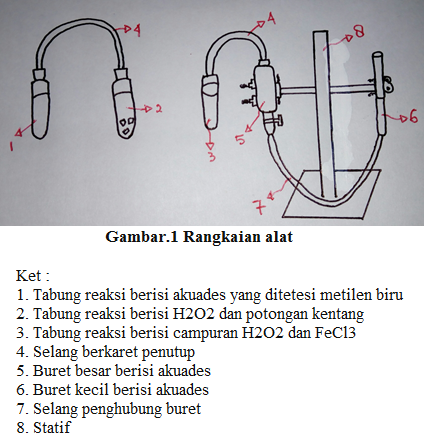
Kenaikkan laju reaksi ini disebabkan dengan kenaikkan suhu atau menyebabkan makin cepatnya molekul molekul pereaksi bergerak sehingga memperbesar kemungkinan terjadi tabrakan yang efektif. Laporan praktikum kimia laju reaksi. Faktor faktor tersebut yaitu konsentrasi suhu luas permukaan dan katalis. Laju reaksi meningkat dengan naiknya suhu biasanya kenaikan suhu sebesar 10 o c akan menyebabkan kenaikkan laju reaksi sebesar dua atau tiga kalinya.